Électrocardiogramme de la tétralogie de Fallot
Auteurs : Eduardo Consuegra Llapur, Ernesto C. Amalfi Aguilera.
La tétralogie de Fallot fut décrite en 1888 par le médecin français Etienne-Louis Arthur Fallot, dont elle porte le nom, bien qu'il soit possible qu'elle ait été décrite bien avant par d'autres auteurs.
Elle est la cardiopathie congénitale cyanogène la plus commune après la première semaine de vie. Sa fréquence d'apparition aux Etats-Unis est d'environ 4 à 5 cas pour 10 000 naissances menées à terme 1 2 3.
Les facteurs qui augmentent le risque de développer une tétralogie de Fallot
Les facteurs qui peuvent augmenter le risque de souffrir de cette cardiopathie congénitale durant la grossesse comprennent :
- Le diabète sucré.
- Une mère âgée de 40 ans ou plus.
- Un alcoolisme prononcé de la part de la mère.
- Une dénutrition durant la grossesse.
On l'associe également à d'autres maladies congénitales telles que les trisomies du chromosome 21 (syndrome de Down), du chromosome 18 (syndrome d'Edwards) 4 ou encore du chromosome 13 (syndrome de Patau). On l'associe aussi au syndrome de Di George et au syndrome d'Alagille.
Composantes de la tétralogie de Fallot
Le terme de “tétralogie” comprend trois composantes anatomiques et l'hypertrophie du ventricule droit, conséquence anatomique de l'obstruction de la chambre de chasse droite provoquée par la sténose pulmonaire.
- Une obstruction de la chambre de chasse du ventricule gauche ou une sténose pulmonaire infundibulaire.
- Une communication interventriculaire.
- Une dextroposition de l’aorte.
- Une hypertrophie concentrique du ventricule droite.
Physiopathologie de la tétralogie de Fallot
La présence d'une sténose pulmonaire cause une augmentation de la pression à l'intérieur du ventricule droit, qui en vient à dépasser la pression du ventricule gauche.
Ce phénomène produit un shunt gauche-droite, où le sang coule depuis le ventricule droit vers le ventricule gauche.
Le sang provenant du ventricule droit, faiblement concentré en oxygène, se mêle au sang du ventricule gauche, oxygéné. Le sang produit de ce mélange est envoyé vers la circulation systémique et devient la cause de la cyanose.
La gravité de la sténose pulmonaire est directement proportionnelle à la taille du shunt gauche-droite et, par conséquent, de la cyanose et est inversement proportionnelle au flux sanguin pulmonaire.
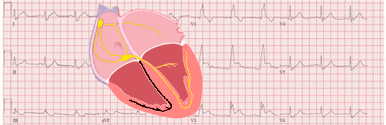
Électrocardiogramme de la tétralogie de Fallot
Chez les nouveaux-nés, l'ECG peut apparaître normal. Néanmoins, dans les premières semaines de vie, on n'observe pas la régression habituelle de la prépondérance du ventricule droit 5.
L'hypertrophie du ventricule droit constitue, d'un point de vue électrocardiographique, le signe distinctif chez les patients souffrant de tétralogie de Fallot. Elle a une grande importance lors du diagnostic différentiel impliquant la communication interventriculaire 5.
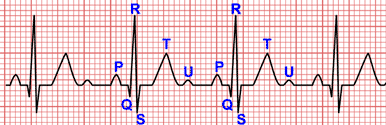
Le signe le plus répandu de l'hypertrophie du ventricule droit est la présence d'ondes R hautes sur les dérivations précordiales droites (V1-V2).
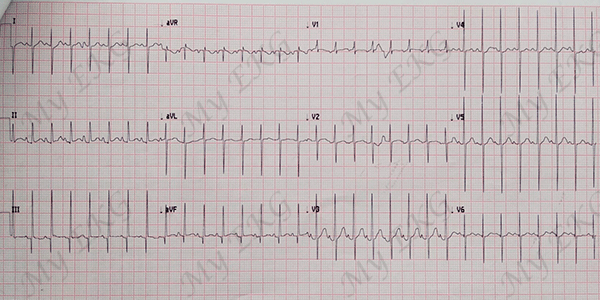
Un patient de 5 jours qui souffre de tétralogie de Fallot :
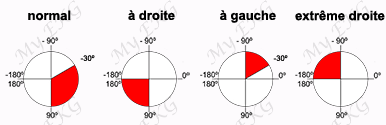
Ondes R hautes sur les dérivations V1 et V2, une transition soudaine (ondes S profondes) sur le dérivation V2. Ondes P hautes, l'axe est normal, à 100° environ.
La déviation axiale droite accompagne généralement l'hypertrophie du ventricule droit. De plus, on peut observer une hypertrophie auriculaire droite sous la forme d'ondes P hautes (P pulmonale).
La présence d'une déviation axiale gauche suggère qu'un canal atrio-ventriculaire y est associé.
Une morphologie fréquemment associée à la tétralogie de Fallot consiste en une transition soudaine de la morphologie des complexes QRS sur les dérivations V1 et V, une morphologie Rs sur V1 et une morphologie rS sur V2 ou V3 qui peut persister jusque sur V6 6.
Références
- 1. Reller MD, Strickland MJ et al. Prevalence of congenital heart defects in metropolitan Atlanta, 1998-2005. J Pediatr. 2008 Dec;153(6):807-13. doi: 10.1016/j.jpeds.2008.05.059.
- 2. Centers for Disease Control and Prevention (CDC). Improved national prevalence estimates for 18 selected major birth defects--United States, 1999-2001. MMWR Morb Mortal Wkly Rep. 2006 Jan 6;54(51):1301-5.
- 3. Allen HD, Gutgesell HP, Clark EB, Dricoll DJ: Moss and Adam’s Heart Disease and Infants, Children and Adolescents Incluiding the Fetus and Young Adult, 6th ed. Philadelphia, PA, Lippincott Williams & Wilkins, 2001.
- 4. Pérez Aytés A, Trisomía 18 (síndrome de Edwards). Protoc diagn ter pediatr. 2010;1:96-100.
- 5. Surawicz B, Knilans TK. Chou’s electrocardiography in clinical practice, 6th ed. Philadelphia: Elservier; 2008.
- 6. Rijnbeek PR, Witsenburg M et al. New normal limits for the paediatric electrocardiogram. Eur Heart J. 2001 Apr;22(8):702-11. doi: 10.1053/euhj.2000.2399
Si ça vous a plu... Partagez-le !